行业标签: 发布时间:2025年03月28天
直接接触药品的包装材料即药品内包材是药品的重要组成部分,关乎药品质量安全乃至消费者的生命健康和安全。全球制药企业均将药品内包材定义为关键物料,并实施严格的供应商审计和质量控制。然而完全按照药品GMP的要求审计内包材制造行业很明显不能兼顾内包材制造工业与制药工业的不同之处 ,因此,ISO15378虽然是自愿性认证产品,但却是全球制药行业和药品内包材制造行业广泛认可并接受的针对直接接触药品的包装材料的GMP规范。
直接接触药品包装材料(简称“药包材”)生产质量管理体系标准ISO15378,它是由国际标准化组织第76个质量技术委员会(ISO/TC 76)先后于2011年、2015年和2017年发布的。ISO15378标准基于药品GMP基本原理,并参照了ISO9001质量管理体系的框架及质量管理原则而制定,是ISO9001质量管理体系在药包材中应用的特殊要求。它充分考虑了药包材生产企业的行业特殊性和产品质量安全的高要求,适用于全世界各地任何规模的组织。
药包材供应链的主要管控要求
为了保证药包材质量可控,安全使用,组织应对如下条件进行适当控制:
►风险评估
风险评估流程能够帮助组织确定潜在威胁,做出正确的决策,进行有效的管理。例如:控制设备的总体需求、员工能力及培训需求、紧急预案及应对措施等。如果没有对控制设备的妥善性及充足性进行风险评估,那么就可能导致控制设备过多或过少地安装,增加无谓的成本支出或影响生产。
►管理体系要素
一套完整的管理体系不仅仅包含了操作程序,也包含了其他支持性要求,例如文件控制(帮忙管理你的文件记录)、方针及目标(确保持续改进)、内部审核(确保体系的监督)、组织架构及职责(明确责任与义务)以及纠正和预防措施(确保事故及体系缺陷能够获得系统化的改正)等。这些体系要素为药包材供应提供了“工具”及平台,确保产品供应体系能够持续改进。
►策划-实施-检查-改进(PDCA)的循环进行
PDCA循环是现代管理的思想流程。在很多组织中,操作程序往往只是单一地执行,缺乏有效的控制。举个典型的例子,某组织在低风险的住宅区安装了先进的视频监控体系(CCTV)(即PDCA中的D),但却没有对此安装行为进行分析和评估(即PDCA中的P),或缺乏对录像设备的维护及检查(即PDCA中的C)。
在PDCA管理体系中,操作程序被视为控制已确认风险的有效手段,可配合有效的监控,确保操作行为的高效执行。
ISO15378标准适用范围
ISO15378标准适用于任何希望保证和展示其符合所声明的质量管理体系方针的药包材设计、生产及供应的组织。同时,也可作为组织的药包材质量管理体系认证、评价及自我声明依据。
药包材可以按材质、用途和形制进行分类。
按材质分类:1.塑料类、2.金属类、3.玻璃类、4.陶瓷类、5.橡胶类、6.其他类(如纸、干燥剂)、7. 1-6项类型的任意组合。
按用途和形制分类:1.输液瓶(袋、膜及配件)、2.安瓿、3.药用(注射剂、口服或者外用剂型)瓶(管、盖)、4.药用胶塞、5.药用预灌封注射器、6.药用滴眼(鼻、耳)剂瓶、7.药用硬片(膜)8.药用铝箔、9.药用软膏管(盒)、10.药用喷(气)雾剂泵(阀门、罐、筒)、11.药用干燥剂等。
一、服务商药包材行业ISO15378之GMP的全面解决方案
1. ISO15378标准通过注重实效的方法,帮助组织确定产品设计、生产和供应运营中的风险级别。在支持性管理工具(如:文件控制、方针及目标、内审及培训)的帮助下,对组织进行风险等级评估,并针对存在的风险实施控制措施。
2. ISO15378标准的结构与ISO9001质量管理体系(QMS)标准的结构相似。但结合了药品GMP特殊要求,加强风险评估、验证与确认过程。
二、服务商关于ISO15378的解决方案
我们可为您提供各种药包材GMP的解决方案,助力组织提升人员的能力及意识。
1. 管理体系
●ISO15378基础知识及意识培训;
●ISO15378 - 药包材GMP法规要求解读;
●ISO15378 - 药包材GMP内审员培训。
2.专题技术类
●风险管理技能;
●设施设备验证与确认;
●车间及库房虫害控制;
●清洁和消毒知识讲解;
●洁净厂房运行及维护技能辅导。
3. 客户定制类
●定制化的药包材GMP-ISO15378管理体系建立和运行的辅导;
●企业现场差距分析(包括预审核及评估);
●定制化的管理技能培训;
●其他应客户要求的定制化解决方案;
●实验室检测和其他相关服务。
服务商的实验室网络提供了多种药品、药包材检测及测试服务和解决方案来帮助你了解产品等质量水平,确保生产过程和整个供应链的质量可控、安全。(具体如下)
✔分析方法开发与验证;
✔药包材兼容性研究;
✔产品无菌测试;
✔微生物限度测试;
✔洁净车间环境监控;
✔仪器检验及性能确认等。
一、确保药包材设计、生产和供应遵守标准要求。
二、提高和改善企业的管理水平,增加企业的知名度。
三、提高和保证产品的质量,使企业获取更大的经济效益。
四、有利于消除贸易壁垒,取得进入国际市场的通行证。
五、有利于增强产品竞争力,提高产品的市场占有率。
六、是向利益相关方展示组织系统性管理已得到加强的有效证明。
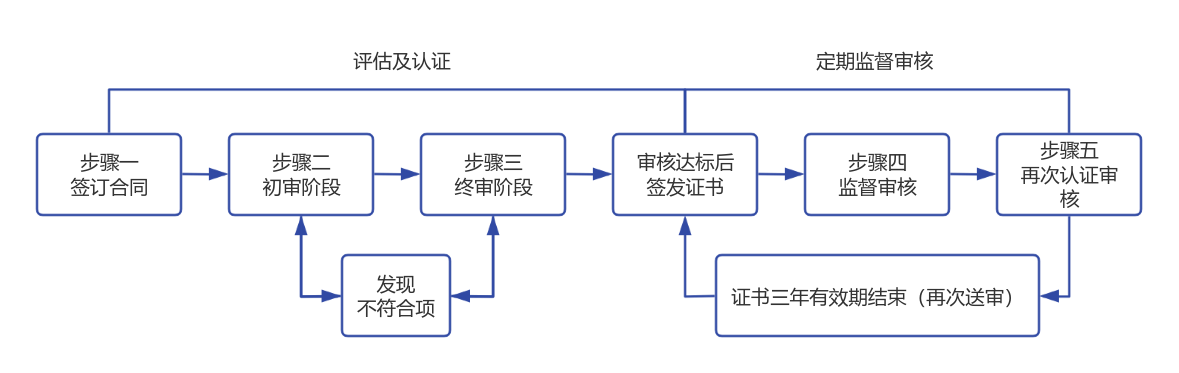
一、具体内容
►步骤6 — 证书签发满3年期后,实施再认证审核。
二、图示
★QAWORKS承诺公平公正公开,拥有权威的审核机制,专业筛选认证服务商,资质真实可靠。
★QAWORKS拥有丰富资源,网络覆盖多个行业领域,平台旗下有60+资深顾问,500+机构及千名专家。
★QAWORKS下合作机构驻扎全国各地,辐射全国超5000家制造企业。
★QAWORKS专业团队为企业优选高性价比机构,解决质量、认证、知识产权等全链问题。
★QAWORKS实时观测行业动态,及时发布专业的行业消息,助力为企业了解行业更加便利。
★QAWORKS为用户提供公开投标服务,透明化市场价格,助力行业良性循环。