行业标签: 发布时间:2025年03月13天
ISO13485明确了有关质量管理体系(QMS)的要求,以帮助组织展示其提供符合用户和法律标准的医疗器械和相关服务的能力。
该组织可以是参与一个或多个生命周期的阶段,包括生产、存储、分发和安装;它还可以是参与维修、设计和开发,或技术支持等相关活动。
无论是对于品牌持有者、小型制造商,还是跨国企业,医疗器械认证均同样适用。
成功通过审核认证后,将帮助组织:
►更快速地生产和分配设备
►获得竞争优势
►促进系统性流程改进
►监控供应链的持续改进
►探索提高效率和增加价值的方法
一、具体内容
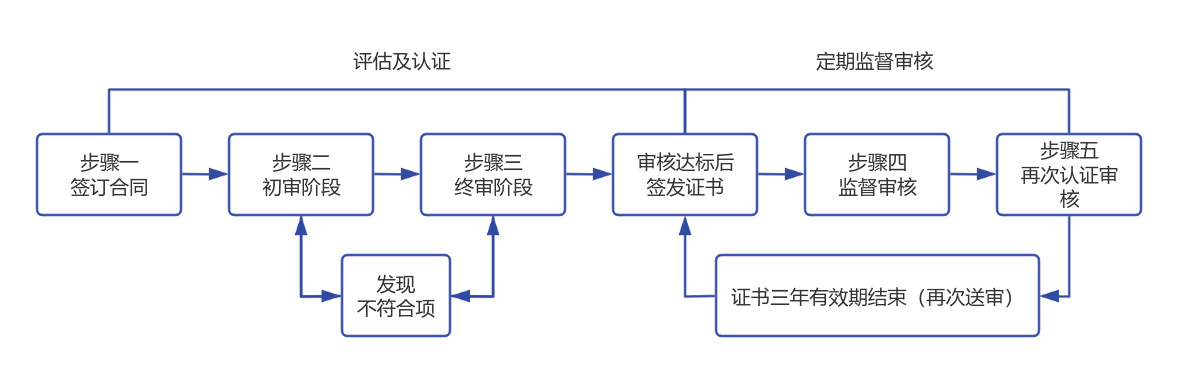
►步骤1 - 服务商依据用户体量及业态制定专属方案,待用户确认建议书后启动审核流程。
►步骤2 - 初审阶段:核查用户文件管理架构及关键流程规范性,提出不符合项。
►步骤3 - 终审阶段:通过人员问询、记录核验及现场实操验证形成评审结果,达标后签发认证证书。
►步骤4 - 按合约周期(半年/年度)对用户体系维护及纠正措施执行跟踪审查。
►步骤5 - 证书三年有效期结束后,需再次认证审核。
二、图示
★QAWORKS承诺公平公正公开,拥有权威的审核机制,专业筛选认证服务商,资质真实可靠。
★QAWORKS拥有丰富资源,网络覆盖多个行业领域,平台旗下有60+资深顾问,500+机构及千名专家。
★QAWORKS下合作机构驻扎全国各地,辐射全国超5000家制造企业。
★QAWORKS专业团队为企业优选高性价比机构,解决质量、认证、知识产权等全链问题。
★QAWORKS实时观测行业动态,及时发布专业的行业消息,助力为企业了解行业更加便利。
★QAWORKS为用户提供公开投标服务,透明化市场价格,助力行业良性循环。